Cada 14 de abril, el Día Mundial del Chagas recuerda la importancia de atender esta en enfermedad que afecta a unos 7 millones de personas en el mundo, principalmente en América Latina. En el instituto, varios laboratorios se dedican a investigar diferentes
aspectos del Chagas y aportan al conocimiento sobre la genómica y el mecanismo de infección.
El Chagas y su silencio
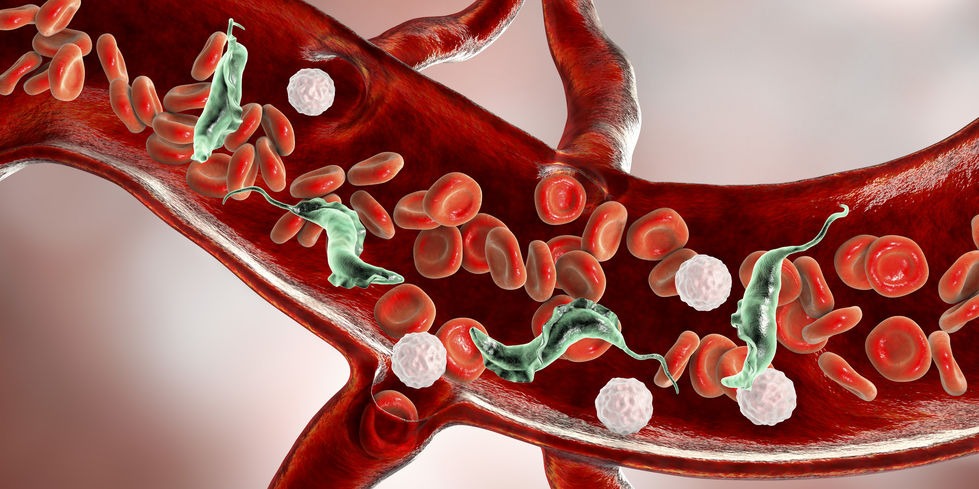
El Chagas es una enfermedad parasitaria potencialmente mortal causada por el parásito Trypanosoma cruzi. Se transmite a las personas y animales a través de la picadura de vinchucas, un insecto que habita zonas rurales y/o donde predominan condiciones de pobreza.
Además de esta vía de transmisión, también puede adquirirse por transfusiones de sangre, trasplantes de órganos, consumo de alimentos contaminados con el parásito, y de madre a hijo por la placenta durante el embarazo.
En el organismo, el parásito se aloja en las células del corazón y del intestino provocando insuficiencia cardíaca, problemas digestivos y riesgo de padecer accidentes cerebrovasculares.
La infección puede causar síntomas leves como cansancio, dolor corporal, pérdida de apetito, vómitos, entre otros, y presentarse sin síntomas durante toda la vida del individuo, lo que ocurre en 70% de los casos. No obstante, 30% podrán desarrollar algún trastorno cardíaco, digestivo o del sistema nervioso que puede ser mortal.
Un escondite intestinal
Una vez que infecta el organismo, Trypanosoma cruzi logra evadir la respuesta de
nuestro sistema inmune y de los fármacos que se utilizan para combatirlo.
Para entender cómo se aloja este parásito especialmente en el intestino, dos grupos del instituto —el Laboratorio de Biología Redox de Tripanosomátidos y la Unidad de Biología Celular— desarrollaron intestinos en miniatura creados en el laboratorio.
Estos “mini órganos” se generaron a partir de células madre que imitan la estructura y función de los órganos y sirven como modelos de investigación para estudiar cómo se forman los tejidos, cómo se desarrollan las enfermedades y cómo funcionan los fármacos, entre otras utilidades.
En su trabajo, los científicos infectaron estos mini intestinos con el patógeno T. cruzi para estudiar dónde y cómo se replica en las células y conocer qué pasa con la acción de los fármacos.
Los resultados del trabajo se publicaron en marzo de 2024 en Frontiers en Microbiology. Este trabajo es liderado por Marcelo Comini y Mariela Bollati, responsables del Laboratorio de Biología Redox de Tripanosomátidos y la Unidad de Biología Celular, respectivamente.
Especializado en placentas
En el instituto, el Laboratorio de Interacciones Hospedero-Patógeno (LIHP) también se dedica al estudio del Chagas, pero observando en particular los casos de embarazadas infectadas.
Este estudio parte de datos recabados por el Departamento de Parasitología y
Micología del Instituto de Higiene de la Universidad de la República que realiza un monitoreo sistemático a las embarazadas con Chagas.
En esos estudios se observó que muchas de las embarazadas con Chagas no tenían síntomas, y al profundizar el análisis familiar se constataba que la infección también estaba presente en la madre de la gestante y en su abuela. Esto implicaba que el parásito lograba transmitirse de manera silenciosa de generación en generación.
A partir de esta observación, científicos del Instituto Pasteur de Montevideo
desarrollaron un estudio que confirmó que las cepas de los parásitos detectadas en las mujeres se habían especializado para transmitirse a través de la placenta. No eran tan virulentas como cepas que se transmiten por otras vías y lograban esa vinculación parasitaria con el organismo de modo silencioso.
Un estudio del LIHP, liderado por Paula Faral y publicado en 2023 en Microbiology Spectrum, analizó características de esas cepas especializadas en transmisión placentaria y halló que mientras que la cepa virulenta de T. cruzi moduló más de 2.500 genes placentarios para ingresar hasta el feto, las cepas especializadas en transmisión vertical solo modularon 150 genes, generando una menor respuesta inmune en el organismo.
Ahora, un nuevo estudio iniciado por el LIHP —liderado por Lisvane Paes— y
financiado por la Agencia Nacional de Investigación e Innovación, busca dar un paso más y secuenciar el genoma de estas cepas especializadas.